Científicos identifican los componentes químicos clave para el medicamento antiviral contra el SARS-CoV-2
|
Por el equipo editorial de HospiMedica en español Actualizado el 13 Jul 2020 |
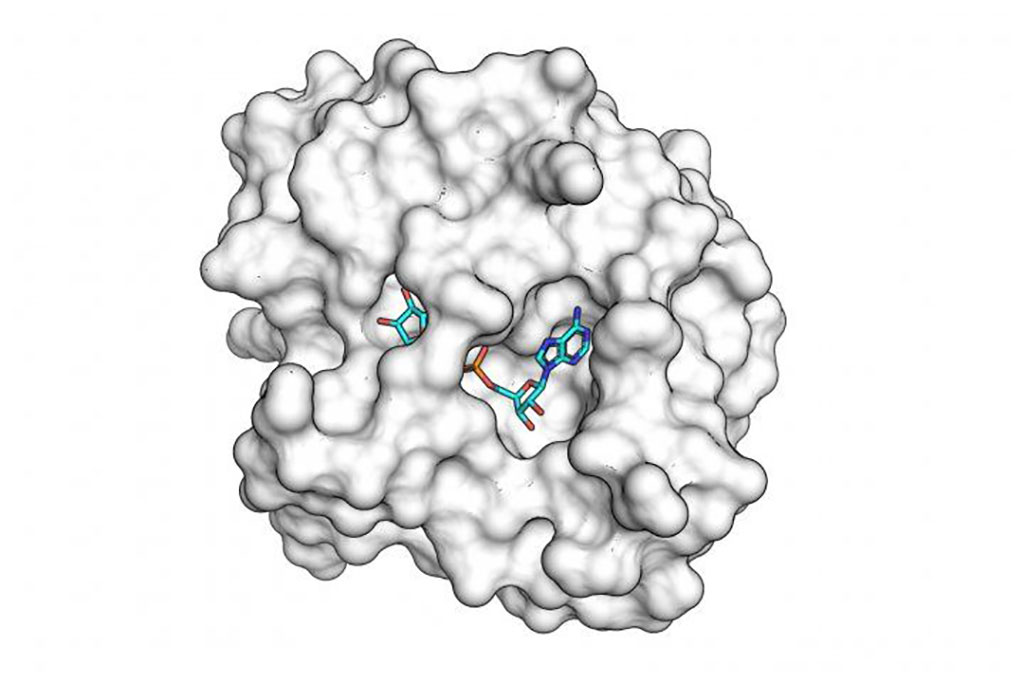
Imagen: La proteína del macrodominio SARS-CoV-2 unida a fragmentos de moléculas pequeñas que podrían ser la base de nuevos medicamentos antivirales (Fotografía cortesía de UCSF)
Un equipo de científicos identificó los componentes químicos clave para un eventual medicamento antiviral contra el SARS-CoV-2.
Los nuevos compuestos, identificados por investigadores del Grupo de Investigación de Coronavirus del Instituto de Cuantitativo de Biociencia de la UC San Francisco (QCRG), en colaboración con el Laboratorio Nacional Lawrence Berkeley (Berkeley Lab) y el Laboratorio Nacional de Aceleradores SLAC (SLAC) se unen a una enzima producida por el virus, llamada el “macrodominio”, que se sabe es crucial para la capacidad del virus de replicarse en las células humanas. El estudio se centró en las enzimas poli (ADP-ribosa) polimerasas (PARP), que desempeñan un papel importante en la reparación del ADN y que han sido objeto de medicamentos para tratar ciertos tipos de cáncer.
Los investigadores se propusieron comprender la estructura molecular del macrodominio para identificar moléculas pequeñas con la forma correcta para atascar el sitio activo de la proteína viral, el primer paso hacia la construcción de un medicamento antiviral que podría inhibir la propagación del virus mediante la repotenciación de las etiquetas protectoras de PARP. Mediante la cristalografía de rayos X, los investigadores cultivaron cristales de proteínas de macrodominio aisladas, luego bombardearon estos cristales con poderosos rayos X, utilizando los patrones de difracción resultantes para inferir una imagen detallada de la estructura atómica del macrodominio hasta una resolución de casi un angstrom, una millonésima parte del diámetro de un cabello humano. Para identificar pequeñas moléculas capaces de unirse al macrodominio, los investigadores utilizaron una técnica llamada “remojo de fragmentos” que implica crear cientos de cristales de macrodominio, luego usar ondas de sonido para manipular moléculas pequeñas candidatas en el corazón de cada cristal y congelarlas juntas en nitrógeno líquido antes de regresar a las fuentes de luz de rayos X para obtener más imágenes. Los experimentos de difracción de rayos X revelaron 13 moléculas pequeñas, cada una de aproximadamente un tercio a un cuarto del tamaño de una molécula de fármaco normal, que se unieron con éxito al macrodominio, incluidas cuatro que se unieron al sitio activo de la enzima.
Con la nueva información sobre qué estructuras químicas pueden unirse de manera efectiva al sitio activo del macrodominio, los investigadores empezaron a trabajar con una plataforma virtual de descubrimiento de fármacos para examinar rápidamente 500 millones de moléculas potenciales similares a fármacos para encontrar candidatos a fármacos que combinen varias de estas estructuras químicas potentes. Según los investigadores, se necesita más trabajo para soldar estos ingredientes activos potenciales en un candidato a fármaco viable, pero la investigación representa una frontera prometedora nueva en la batalla contra el virus, particularmente debido a las incertidumbres sobre el momento o la eficacia final de una vacuna eventual. Los investigadores publicaron sus datos directamente en línea para acelerar los esfuerzos mundiales para combatir la pandemia de coronavirus.
“El macrodominio SARS-CoV-2 no se entiende tan bien como la proteasa principal del virus o las proteínas spike que han sido mucho más estudiadas”, dijo James Fraser, PhD, profesor asociado en el Departamento de Bioingeniería y Ciencias Terapéuticas en las facultades de Farmacia y Medicina de la UCSF, quienes lideraron el esfuerzo de investigación como parte del Consorcio de Biología Estructural QCRG en la UCSF. “Queríamos estudiar campos que los otros no investigaban tan fuertemente y logramos identificar a algunos candidatos prometedores para crear medicamentos que podrían detener la capacidad del virus para replicarse y extenderse en el cuerpo humano”.
Enlace relacionado:
Los nuevos compuestos, identificados por investigadores del Grupo de Investigación de Coronavirus del Instituto de Cuantitativo de Biociencia de la UC San Francisco (QCRG), en colaboración con el Laboratorio Nacional Lawrence Berkeley (Berkeley Lab) y el Laboratorio Nacional de Aceleradores SLAC (SLAC) se unen a una enzima producida por el virus, llamada el “macrodominio”, que se sabe es crucial para la capacidad del virus de replicarse en las células humanas. El estudio se centró en las enzimas poli (ADP-ribosa) polimerasas (PARP), que desempeñan un papel importante en la reparación del ADN y que han sido objeto de medicamentos para tratar ciertos tipos de cáncer.
Los investigadores se propusieron comprender la estructura molecular del macrodominio para identificar moléculas pequeñas con la forma correcta para atascar el sitio activo de la proteína viral, el primer paso hacia la construcción de un medicamento antiviral que podría inhibir la propagación del virus mediante la repotenciación de las etiquetas protectoras de PARP. Mediante la cristalografía de rayos X, los investigadores cultivaron cristales de proteínas de macrodominio aisladas, luego bombardearon estos cristales con poderosos rayos X, utilizando los patrones de difracción resultantes para inferir una imagen detallada de la estructura atómica del macrodominio hasta una resolución de casi un angstrom, una millonésima parte del diámetro de un cabello humano. Para identificar pequeñas moléculas capaces de unirse al macrodominio, los investigadores utilizaron una técnica llamada “remojo de fragmentos” que implica crear cientos de cristales de macrodominio, luego usar ondas de sonido para manipular moléculas pequeñas candidatas en el corazón de cada cristal y congelarlas juntas en nitrógeno líquido antes de regresar a las fuentes de luz de rayos X para obtener más imágenes. Los experimentos de difracción de rayos X revelaron 13 moléculas pequeñas, cada una de aproximadamente un tercio a un cuarto del tamaño de una molécula de fármaco normal, que se unieron con éxito al macrodominio, incluidas cuatro que se unieron al sitio activo de la enzima.
Con la nueva información sobre qué estructuras químicas pueden unirse de manera efectiva al sitio activo del macrodominio, los investigadores empezaron a trabajar con una plataforma virtual de descubrimiento de fármacos para examinar rápidamente 500 millones de moléculas potenciales similares a fármacos para encontrar candidatos a fármacos que combinen varias de estas estructuras químicas potentes. Según los investigadores, se necesita más trabajo para soldar estos ingredientes activos potenciales en un candidato a fármaco viable, pero la investigación representa una frontera prometedora nueva en la batalla contra el virus, particularmente debido a las incertidumbres sobre el momento o la eficacia final de una vacuna eventual. Los investigadores publicaron sus datos directamente en línea para acelerar los esfuerzos mundiales para combatir la pandemia de coronavirus.
“El macrodominio SARS-CoV-2 no se entiende tan bien como la proteasa principal del virus o las proteínas spike que han sido mucho más estudiadas”, dijo James Fraser, PhD, profesor asociado en el Departamento de Bioingeniería y Ciencias Terapéuticas en las facultades de Farmacia y Medicina de la UCSF, quienes lideraron el esfuerzo de investigación como parte del Consorcio de Biología Estructural QCRG en la UCSF. “Queríamos estudiar campos que los otros no investigaban tan fuertemente y logramos identificar a algunos candidatos prometedores para crear medicamentos que podrían detener la capacidad del virus para replicarse y extenderse en el cuerpo humano”.
Enlace relacionado:
Últimas COVID-19 noticias
- Sistema de bajo costo detecta el virus SARS-CoV-2 en el aire del hospital mediante burbujas de alta tecnología
- China aprueba la primera vacuna inhalable contra la COVID-19 del mundo
- Vacuna en parche contra la COVID-19 combate variantes del SARS-CoV-2 mejor que las agujas
- Pruebas de viscosidad sanguínea predicen riesgo de muerte en pacientes hospitalizados con COVID-19
- ‘Computadora Covid’ usa IA para detectar COVID-19 en exámenes de TC de tórax
- Técnica de resonancia magnética muestra la causa de los síntomas de COVID prolongada
- TC del tórax de los pacientes con COVID-19 podrían ayudar a diferenciar entre las variantes del SARS-CoV-2
- Resonancia magnética especializada detecta anormalidades pulmonares en pacientes no hospitalizados con COVID prolongada
- Algoritmo de IA identifica a los pacientes hospitalizados con mayor riesgo de morir por COVID-19
- Estudio evalúa el impacto de la COVID-19 sobre la gammagrafía de ventilación/perfusión
- Sensor de sudor detecta biomarcadores claves que suministran una alarma precoz de la COVID-19 y la influenza
- Modelo de IA para seguimiento de COVID-19 predice mortalidad durante los primeros 30 días del ingreso
- ECG puede señalar pacientes hospitalizados con COVID-19 con riesgo más alto de muerte
- IA predice pronóstico de COVID a un nivel casi experto con base en tomografías computarizadas
- Examen de TC muestra evidencia de daño pulmonar persistente mucho tiempo después de neumonía por COVID-19
- Plataforma órgano-en-un-chip ayuda a diseñar estrategia para tratar complicaciones severas de la COVID-19
Canales
Cuidados Criticos
ver canal
Nueva tecnología podría revolucionar atención de valvulopatías cardíacas
La valvulopatía, que afecta la función de cualquiera de las cuatro válvulas del corazón, impacta al 2,5 % de la población estadounidense y al 13 % de las personas de... Más
Dispositivo electrónico portátil súper permeable permite monitorear bioseñales a largo plazo
Los dispositivos electrónicos portátiles se han convertido en una parte integral de la mejora de la salud y el estado físico al ofrecer un seguimiento continuo de señales f... Más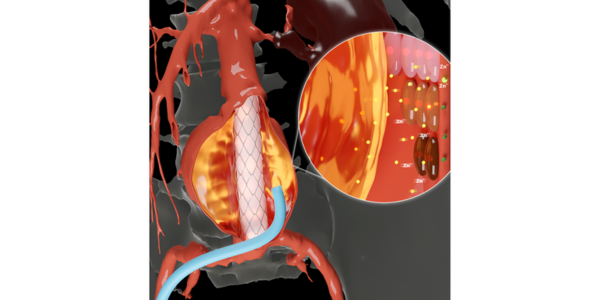
Nuevo hidrogel con capacidades mejoradas para tratar aneurismas y detener su progresión
Los aneurismas pueden desarrollarse en vasos sanguíneos de diferentes áreas del cuerpo, a menudo como resultado de aterosclerosis, infecciones, enfermedades inflamatorias y otros factores de riesgo.... MásNueva herramienta de IA predice eventos médicos para respaldar toma de decisiones clínicas en entornos de atención médica
En un nuevo estudio, los investigadores han demostrado el potencial de una nueva herramienta de inteligencia artificial (IA) para pronosticar la trayectoria de salud de un paciente mediante la predicción... MásTécnicas Quirúrgicas
ver canal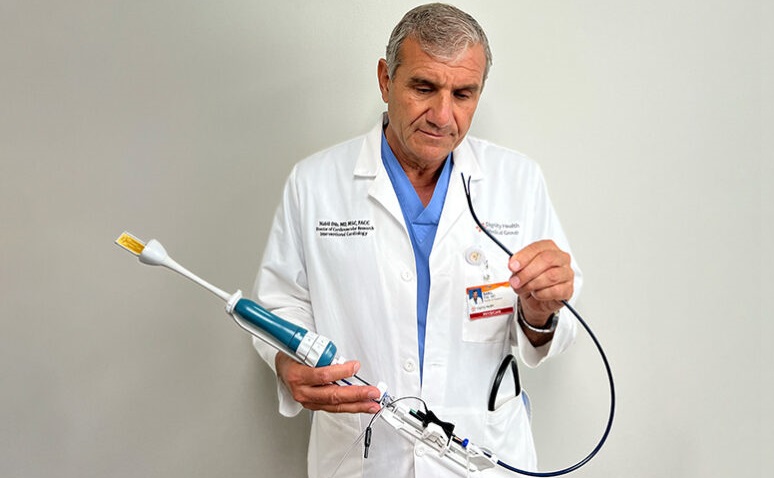
Nuevo sistema de catéter permite procedimientos transeptales más seguros y rentables
En 2021, los cardiólogos realizaron alrededor de 375.000 procedimientos transeptales del corazón izquierdo en los EUA, incluidos cierres, valvuloplastia, reparaciones, septostomías... Más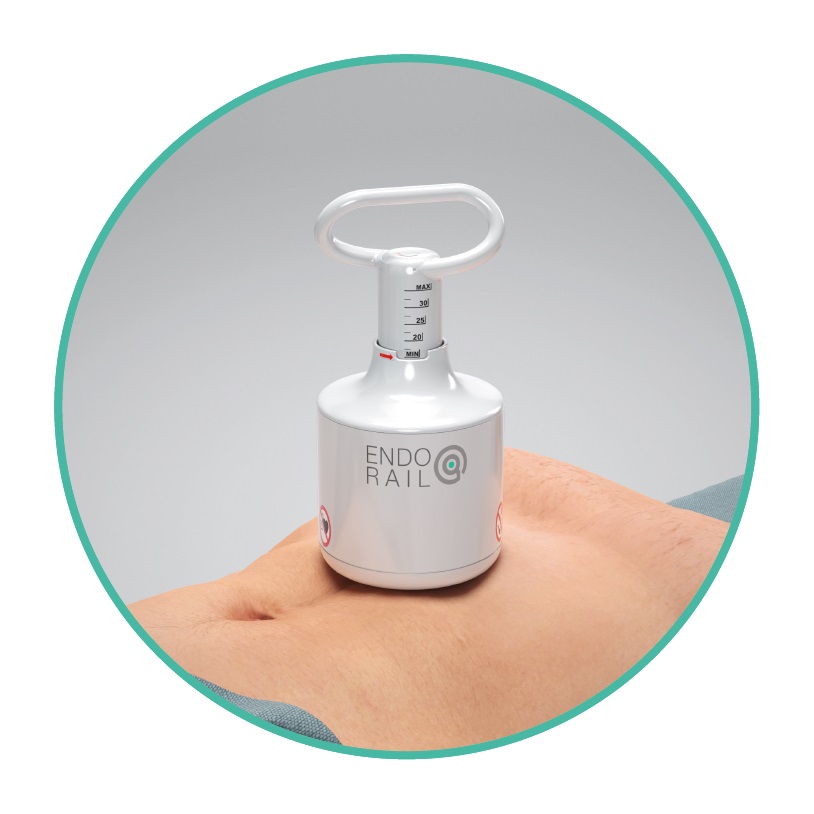
Tecnología de balón magnético optimiza resultados del procedimiento de colonoscopia
La colonoscopia es un procedimiento clave para diagnosticar, monitorear, prevenir y tratar diversas afecciones del colon, como el cáncer colorrectal y las enfermedades inflamatorias intestinales... Más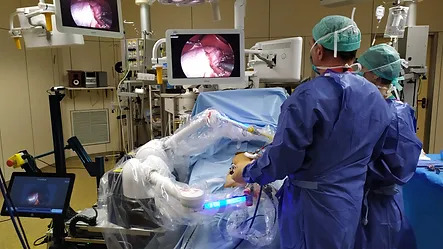
Sistema de cirugía robótica con capacidad basada en visión por computadora allana el camino para laparoscopia de próxima generación
La laparoscopia es una técnica quirúrgica en la que los cirujanos operan a través de pequeñas incisiones con una cámara interna e instrumentos. Ahora, una novedosa t... MásCuidados de Pacientes
ver canal
Solución de optimización de la capacidad quirúrgica ayuda a hospitales a impulsar utilización de quirófanos
Una solución innovadora tiene la capacidad de transformar la utilización de la capacidad quirúrgica al atacar la causa raíz de las ineficiencias los bloques de tiempo quirúrgico.... Más
Innovación revolucionaria en esterilización de instrumentos quirúrgicos mejora significativamente rendimiento del quirófano
Una innovación revolucionaria permite a los hospitales mejorar significativamente el tiempo de procesamiento de instrumentos y el rendimiento en quirófanos y departamentos de procesamiento... Más
Cama para UCI de próxima generación ayuda a abordar necesidades complejas de cuidados intensivos
A medida que el entorno de cuidados intensivos se vuelve cada vez más exigente y complejo debido a las cambiantes necesidades de los hospitales, existe una necesidad apremiante de innovaciones que... MásTI
ver canal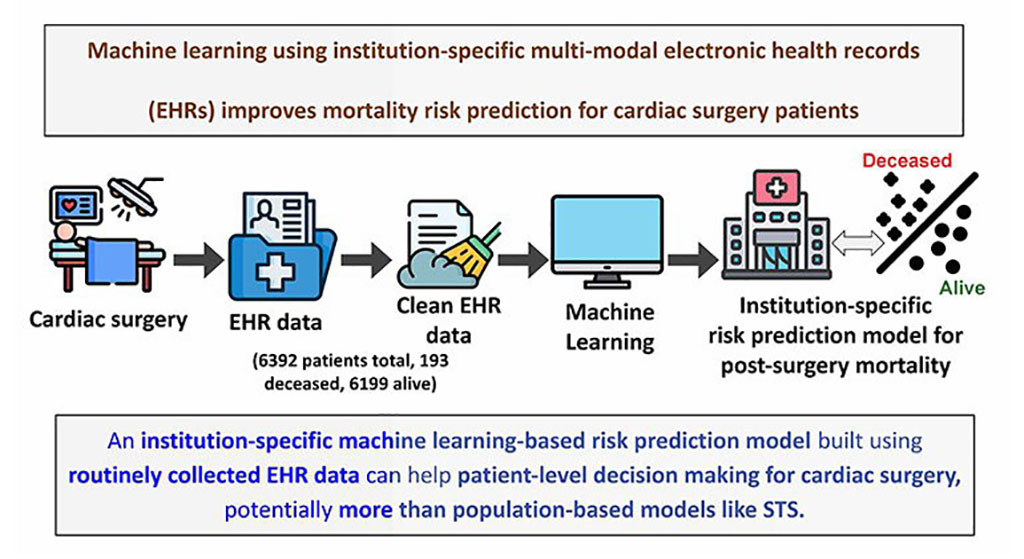
Modelo de aprendizaje automático mejora predicción del riesgo de mortalidad para pacientes de cirugía cardíaca
Se han implementado algoritmos de aprendizaje automático para crear modelos predictivos en varios campos médicos, y algunos han demostrado mejores resultados en comparación con sus... Más
Colaboración estratégica para desarrollar e integrar IA generativa en el cuidado de la salud
Los más altos expertos de la industria han subrayado el requisito inmediato de que los sistemas de salud y los hospitales respondan a las severas presiones de costos y márgenes.... MásPruebas POC
ver canal
Lector de inmunoensayo de pruebas POC proporciona análisis cuantitativo de kits de prueba para diagnóstico más preciso
Un lector de inmunoensayos cuantitativos pequeño y liviano que proporciona un análisis cuantitativo de cualquier tipo de kits o tiras de prueba rápida, y se puede conectar a una PC... Más
Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
Las pruebas hemostáticas actuales proporcionan solo un subconjunto de la información necesaria, o tardan demasiado en ser útiles en situaciones críticas de hemorragia, lo que... Más
Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
La resistencia a los antimicrobianos (RAM) es la falta de respuesta de las bacterias a un determinado antibiótico debido a mutaciones o genes de resistencia que la especie ha adquirido.... MásNegocios
ver canal
Mindray adquirirá empresa china de dispositivos médicos APT Medical
Un reciente análisis exhaustivo de la industria ha demostrado que el mercado cardiovascular mundial ha alcanzado una valoración de 56 mil millones de dólares. En particular, el segmento... Más