Terapia con anticuerpos neutralizantes de Eli Lilly para la COVID-19 reduce las tasas de hospitalización en el ensayo clínico de fase 2
|
Por el equipo editorial de HospiMedica en español Actualizado el 21 Sep 2020 |

Imagen: La terapia con anticuerpos neutralizantes de Eli Lilly para la COVID-19 reduce las tasas de hospitalización en el ensayo clínico de fase 2 (Fotografía cortesía de Eli Lilly and Company)
Se ha descubierto que un anticuerpo neutralizante del SARS-CoV-2, de Eli Lilly and Company (Indianápolis, Indiana, EUA), reduce las tasas de hospitalización entre los pacientes con COVID-19 en un ensayo clínico de fase 2.
Lilly anunció los datos de prueba de concepto de un análisis intermedio del ensayo clínico BLAZE-1, que mostró una tasa reducida de hospitalización para pacientes tratados con LY-CoV555, un anticuerpo neutralizante del SARS-CoV-2. El estudio de fase 2 aleatorizado, doble ciego y controlado con placebo, evaluó LY-CoV555 para el tratamiento de la COVID-19 sintomática en el ámbito ambulatorio. El ensayo reclutó a pacientes con COVID-19 con diagnóstico reciente de leve a moderado en cuatro grupos (placebo, 700 mg, 2800 mg y 7000 mg).
El criterio de valoración principal preespecificado, el cambio desde el inicio en la carga viral en el día 11, se alcanzó en el nivel de dosis de 2800 mg, pero no en los demás. La mayoría de los pacientes, incluidos los que recibieron placebo, demostraron una depuración viral casi completa en el día 11. Los análisis adicionales de los datos virales demostraron que LY-CoV555 mejoró la depuración viral en un momento anterior (día 3) y redujo la proporción de pacientes con una carga viral persistentemente alta en momentos posteriores.
Estos datos de biomarcadores se correlacionaron con el impacto positivo de LY-CoV555 en el criterio de valoración preespecificado de hospitalización o consulta a urgencias relacionada con la COVID-19. Este criterio de valoración se produjo en el 1,7% (5/302) de los pacientes con LY-CoV555, agrupados entre los grupos de dosis, en comparación con el 6% (9/150) de los pacientes con placebo, lo que corresponde a una reducción del riesgo del 72% en esta población limitada. La mayoría de las hospitalizaciones del estudio ocurrieron en pacientes con factores de riesgo subyacentes (edad o IMC), lo que sugiere un efecto del tratamiento más pronunciado para los pacientes de estos grupos de mayor riesgo. En todos los grupos de tratamiento (incluido el placebo), ningún paciente progresó a la ventilación mecánica ni murió. Los análisis exploratorios indicaron una mejoría más rápida de los síntomas en los pacientes tratados con LY-CoV555 en comparación con el placebo, lo que respalda el efecto de la hospitalización.
LY-CoV555 fue bien tolerado y no se informaron eventos adversos graves relacionados con el fármaco. Los eventos adversos emergentes del tratamiento fueron similares en todos los grupos de dosis y comparables a los del placebo. La secuenciación del ARN viral reveló variantes putativas de resistencia a LY-CoV555 en el placebo y en todos los grupos de tratamiento. La tasa de variantes de resistencia fue numéricamente mayor en los pacientes tratados (8%) que en el placebo (6%).
Lilly tiene la intención de publicar rápidamente los resultados de este análisis intermedio en una revista revisada por pares y discutir los próximos pasos apropiados con los reguladores globales. El ensayo clínico BLAZE-1 sigue en curso, demostrando que LY-CoV555 en combinación con un segundo anticuerpo de Lilly, LY-CoV016, que se une a un epítope diferente en la región Spike del SARS-CoV-2. El ensayo inscribe actualmente una cohorte confirmatoria más grande de pacientes de mayor riesgo, probando la capacidad de la combinación de anticuerpos para reducir el número de pacientes con una carga viral persistentemente alta y reducir las hospitalizaciones relacionadas con la COVID-19.
“Estos datos provisionales del ensayo BLAZE-1 sugieren que LY-CoV555, un anticuerpo específicamente dirigido contra el SARS-CoV-2, tiene un efecto antiviral directo y puede reducir las hospitalizaciones relacionadas con la COVID-19”, dijo Daniel Skovronsky, MD, Ph.D., director científico de Lilly y presidente de Lilly Research Laboratories. “Los resultados refuerzan nuestra convicción de que los anticuerpos neutralizantes pueden ayudar en la lucha contra la COVID-19”.
Enlace relacionado:
Eli Lilly and Company
Lilly anunció los datos de prueba de concepto de un análisis intermedio del ensayo clínico BLAZE-1, que mostró una tasa reducida de hospitalización para pacientes tratados con LY-CoV555, un anticuerpo neutralizante del SARS-CoV-2. El estudio de fase 2 aleatorizado, doble ciego y controlado con placebo, evaluó LY-CoV555 para el tratamiento de la COVID-19 sintomática en el ámbito ambulatorio. El ensayo reclutó a pacientes con COVID-19 con diagnóstico reciente de leve a moderado en cuatro grupos (placebo, 700 mg, 2800 mg y 7000 mg).
El criterio de valoración principal preespecificado, el cambio desde el inicio en la carga viral en el día 11, se alcanzó en el nivel de dosis de 2800 mg, pero no en los demás. La mayoría de los pacientes, incluidos los que recibieron placebo, demostraron una depuración viral casi completa en el día 11. Los análisis adicionales de los datos virales demostraron que LY-CoV555 mejoró la depuración viral en un momento anterior (día 3) y redujo la proporción de pacientes con una carga viral persistentemente alta en momentos posteriores.
Estos datos de biomarcadores se correlacionaron con el impacto positivo de LY-CoV555 en el criterio de valoración preespecificado de hospitalización o consulta a urgencias relacionada con la COVID-19. Este criterio de valoración se produjo en el 1,7% (5/302) de los pacientes con LY-CoV555, agrupados entre los grupos de dosis, en comparación con el 6% (9/150) de los pacientes con placebo, lo que corresponde a una reducción del riesgo del 72% en esta población limitada. La mayoría de las hospitalizaciones del estudio ocurrieron en pacientes con factores de riesgo subyacentes (edad o IMC), lo que sugiere un efecto del tratamiento más pronunciado para los pacientes de estos grupos de mayor riesgo. En todos los grupos de tratamiento (incluido el placebo), ningún paciente progresó a la ventilación mecánica ni murió. Los análisis exploratorios indicaron una mejoría más rápida de los síntomas en los pacientes tratados con LY-CoV555 en comparación con el placebo, lo que respalda el efecto de la hospitalización.
LY-CoV555 fue bien tolerado y no se informaron eventos adversos graves relacionados con el fármaco. Los eventos adversos emergentes del tratamiento fueron similares en todos los grupos de dosis y comparables a los del placebo. La secuenciación del ARN viral reveló variantes putativas de resistencia a LY-CoV555 en el placebo y en todos los grupos de tratamiento. La tasa de variantes de resistencia fue numéricamente mayor en los pacientes tratados (8%) que en el placebo (6%).
Lilly tiene la intención de publicar rápidamente los resultados de este análisis intermedio en una revista revisada por pares y discutir los próximos pasos apropiados con los reguladores globales. El ensayo clínico BLAZE-1 sigue en curso, demostrando que LY-CoV555 en combinación con un segundo anticuerpo de Lilly, LY-CoV016, que se une a un epítope diferente en la región Spike del SARS-CoV-2. El ensayo inscribe actualmente una cohorte confirmatoria más grande de pacientes de mayor riesgo, probando la capacidad de la combinación de anticuerpos para reducir el número de pacientes con una carga viral persistentemente alta y reducir las hospitalizaciones relacionadas con la COVID-19.
“Estos datos provisionales del ensayo BLAZE-1 sugieren que LY-CoV555, un anticuerpo específicamente dirigido contra el SARS-CoV-2, tiene un efecto antiviral directo y puede reducir las hospitalizaciones relacionadas con la COVID-19”, dijo Daniel Skovronsky, MD, Ph.D., director científico de Lilly y presidente de Lilly Research Laboratories. “Los resultados refuerzan nuestra convicción de que los anticuerpos neutralizantes pueden ayudar en la lucha contra la COVID-19”.
Enlace relacionado:
Eli Lilly and Company
Últimas COVID-19 noticias
- Sistema de bajo costo detecta el virus SARS-CoV-2 en el aire del hospital mediante burbujas de alta tecnología
- China aprueba la primera vacuna inhalable contra la COVID-19 del mundo
- Vacuna en parche contra la COVID-19 combate variantes del SARS-CoV-2 mejor que las agujas
- Pruebas de viscosidad sanguínea predicen riesgo de muerte en pacientes hospitalizados con COVID-19
- ‘Computadora Covid’ usa IA para detectar COVID-19 en exámenes de TC de tórax
- Técnica de resonancia magnética muestra la causa de los síntomas de COVID prolongada
- TC del tórax de los pacientes con COVID-19 podrían ayudar a diferenciar entre las variantes del SARS-CoV-2
- Resonancia magnética especializada detecta anormalidades pulmonares en pacientes no hospitalizados con COVID prolongada
- Algoritmo de IA identifica a los pacientes hospitalizados con mayor riesgo de morir por COVID-19
- Estudio evalúa el impacto de la COVID-19 sobre la gammagrafía de ventilación/perfusión
- Sensor de sudor detecta biomarcadores claves que suministran una alarma precoz de la COVID-19 y la influenza
- Modelo de IA para seguimiento de COVID-19 predice mortalidad durante los primeros 30 días del ingreso
- ECG puede señalar pacientes hospitalizados con COVID-19 con riesgo más alto de muerte
- IA predice pronóstico de COVID a un nivel casi experto con base en tomografías computarizadas
- Examen de TC muestra evidencia de daño pulmonar persistente mucho tiempo después de neumonía por COVID-19
- Plataforma órgano-en-un-chip ayuda a diseñar estrategia para tratar complicaciones severas de la COVID-19
Canales
Cuidados Criticos
ver canal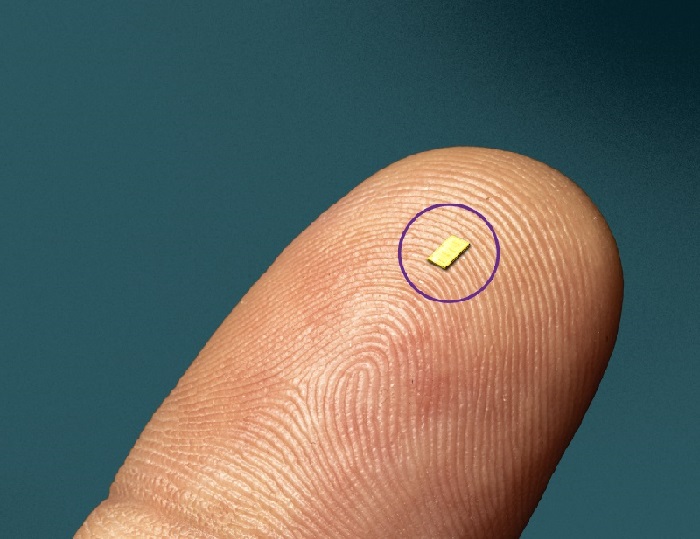
Tecnología innovadora combina detección y tratamiento de trastornos del sistema nervioso en un solo procedimiento.
El sistema nervioso periférico (SNP) sirve como red de comunicación que conecta el cerebro y la médula espinal con todas las demás partes del cuerpo. Consta de dos partes: el... Más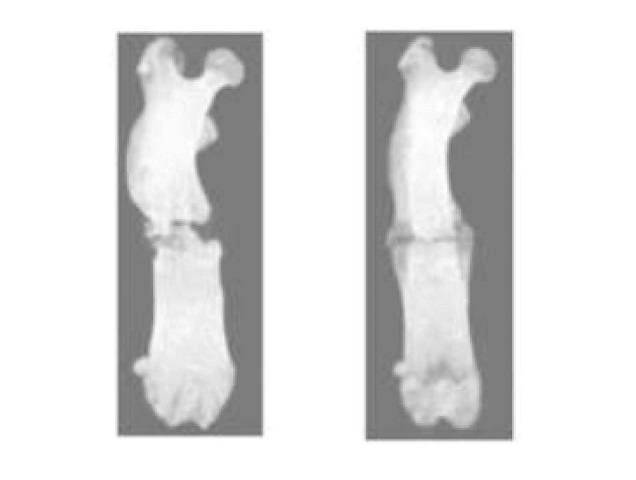
Irradiación de plasma promueve una cicatrización ósea más rápida
Si bien la mayoría de las fracturas óseas sanan adecuadamente, alrededor del 5 % al 10 % no lo hacen, lo que provoca retrasos en la consolidación o pseudoartrosis que pueden causar... MásTécnicas Quirúrgicas
ver canal
Plataforma de imágenes de vanguardia detecta cáncer de mama residual que no se detectó durante la cirugía de lumpectomía
El cáncer de mama es cada vez más común y las estadísticas indican que 1 de cada 8 mujeres desarrollará la enfermedad a lo largo de su vida. La lumpectomía sigue... Más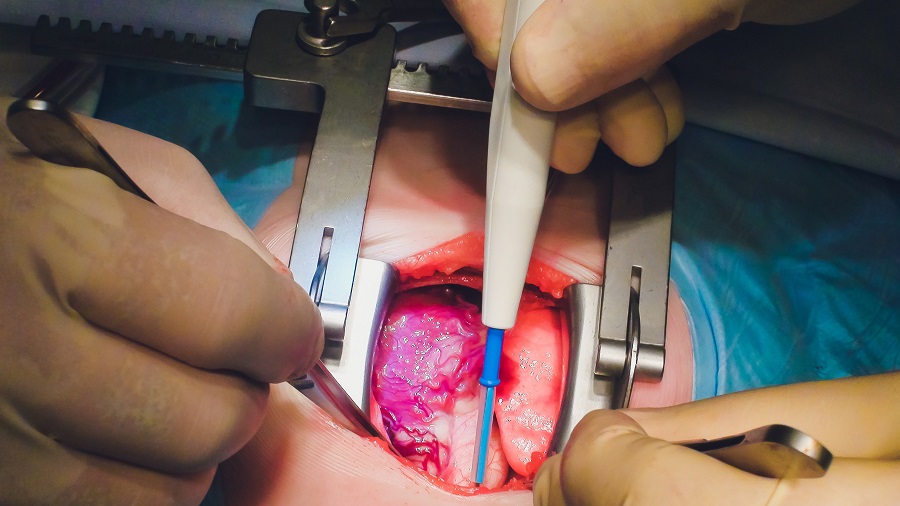
Modelos computacionales predicen la fuga de válvulas cardíacas en niños
El síndrome del corazón izquierdo hipoplásico es un defecto congénito grave en el que el lado izquierdo del corazón de un bebé está subdesarrollado y es... Más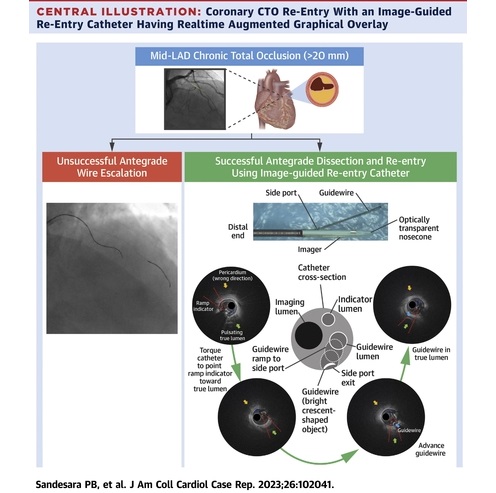
Dispositivo innovador permite orientación visual clara y en tiempo real para intervenciones cardiovasculares efectivas
La oclusión total crónica coronaria (OCT) es una afección en la que una arteria coronaria queda completamente bloqueada debido a la acumulación de placa. Aproximadamente entre... MásCuidados de Pacientes
ver canal
Solución de optimización de la capacidad quirúrgica ayuda a hospitales a impulsar utilización de quirófanos
Una solución innovadora tiene la capacidad de transformar la utilización de la capacidad quirúrgica al atacar la causa raíz de las ineficiencias los bloques de tiempo quirúrgico.... Más
Innovación revolucionaria en esterilización de instrumentos quirúrgicos mejora significativamente rendimiento del quirófano
Una innovación revolucionaria permite a los hospitales mejorar significativamente el tiempo de procesamiento de instrumentos y el rendimiento en quirófanos y departamentos de procesamiento... Más
Cama para UCI de próxima generación ayuda a abordar necesidades complejas de cuidados intensivos
A medida que el entorno de cuidados intensivos se vuelve cada vez más exigente y complejo debido a las cambiantes necesidades de los hospitales, existe una necesidad apremiante de innovaciones que... MásTI
ver canal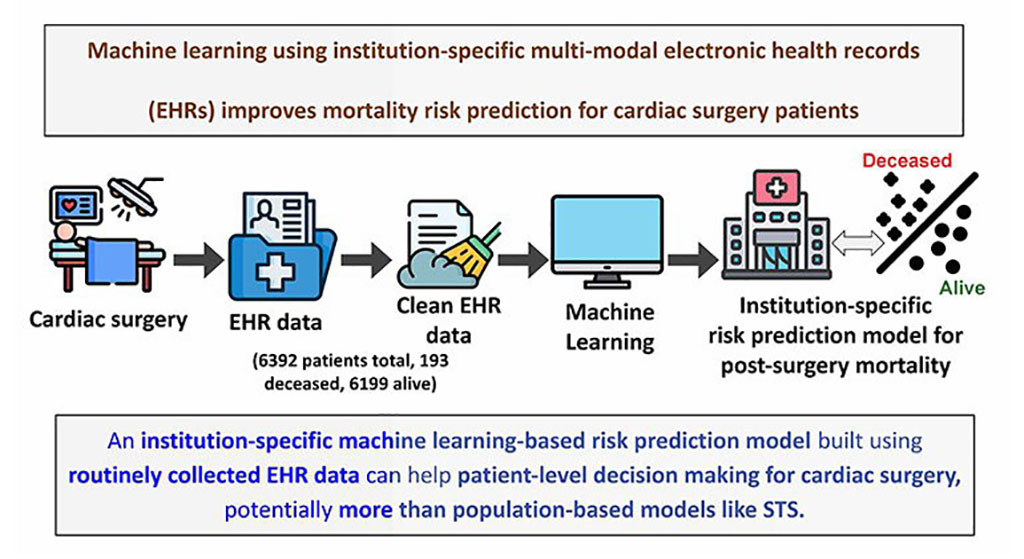
Modelo de aprendizaje automático mejora predicción del riesgo de mortalidad para pacientes de cirugía cardíaca
Se han implementado algoritmos de aprendizaje automático para crear modelos predictivos en varios campos médicos, y algunos han demostrado mejores resultados en comparación con sus... Más
Colaboración estratégica para desarrollar e integrar IA generativa en el cuidado de la salud
Los más altos expertos de la industria han subrayado el requisito inmediato de que los sistemas de salud y los hospitales respondan a las severas presiones de costos y márgenes.... MásPruebas POC
ver canal
Lector de inmunoensayo de pruebas POC proporciona análisis cuantitativo de kits de prueba para diagnóstico más preciso
Un lector de inmunoensayos cuantitativos pequeño y liviano que proporciona un análisis cuantitativo de cualquier tipo de kits o tiras de prueba rápida, y se puede conectar a una PC... Más
Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
Las pruebas hemostáticas actuales proporcionan solo un subconjunto de la información necesaria, o tardan demasiado en ser útiles en situaciones críticas de hemorragia, lo que... Más
Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
La resistencia a los antimicrobianos (RAM) es la falta de respuesta de las bacterias a un determinado antibiótico debido a mutaciones o genes de resistencia que la especie ha adquirido.... MásNegocios
ver canal
Johnson & Johnson adquiere la empresa de dispositivos médicos cardiovasculares Shockwave Medical
Johnson & Johnson (New Brunswick, Nueva Jersey, EUA) y Shockwave Medical (Santa Clara, CA, EUA.) han firmado un acuerdo definitivo en virtud del cual Johnson & Johnson adquirirá todas las... Más