Aplicación IND de Pluristem para el estudio en fase II de células PLX para tratamiento de la COVID-19 recibe aprobación de la FDA
|
Por el equipo editorial de HospiMedica en español Actualizado el 12 May 2020 |
Ilustración
Pluristem Therapeutics Inc. (Haifa, Israel) recibió la autorización de la FDA de los EUA para su aplicación de Nueva Droga en Investigación (IND, por su sigla en inglés) para un estudio de fase II de sus células PLX en el tratamiento de casos graves de COVID-19 complicados por el Síndrome de Dificultad Respiratoria Aguda (SDRA).
Las células PLX son células alogénicas de tipo mesenquimatoso que tienen propiedades inmunomoduladoras que inducen las células T reguladoras naturales del sistema inmune y los macrófagos M2 y, por lo tanto, pueden prevenir o revertir la activación exagerada peligrosa del sistema inmune. Los hallazgos preclínicos previos de las células PLX revelaron un beneficio terapéutico en estudios con animales de hipertensión pulmonar, fibrosis pulmonar, lesión renal aguda y lesión gastrointestinal, que son posibles complicaciones de la infección grave por COVID-19. Los datos clínicos con el uso de células PLX demostraron la fuerte potencia inmunomoduladora de las células PLX en pacientes después de una cirugía importante.
Las celdas PLX están disponibles en el mercado y una vez comercializadas, se pueden fabricar en grandes cantidades. Pluristem cree que sus células PLX ofrecerán una ventaja clave para abordar la pandemia global de COVID-19. Las células PLX podrían reducir potencialmente la incidencia y/o la gravedad de la neumonía y neumonitis por COVID-19, lo que con suerte mejoraría el pronóstico de los pacientes. Las capacidades potenciales de las células PLX, junto con el perfil de seguridad observado en los ensayos clínicos que involucran a cientos de pacientes en todo el mundo, las posicionan potencialmente como una terapia para mitigar los efectos dañinos de la COVID-19 en los tejidos.
El estudio de fase II, titulado “Un estudio aleatorizado de fase II, doble ciego, controlado con placebo, multicéntrico, de grupos paralelos, para evaluar la eficacia y seguridad de las inyecciones intramusculares de PLX-PAD para el tratamiento de COVID-19 grave” tratará 140 pacientes adultos intubados y ventilados mecánicamente y que sufren insuficiencia respiratoria y SDRA debido a COVID-19. El criterio de valoración principal de eficacia del estudio es el número de días sin ventilador durante los 28 días desde el día uno hasta el día 28 del estudio.
El objetivo del estudio es evaluar la eficacia y seguridad de una o dos inyecciones intramusculares (IM), en tres dosis diferentes, de PLX-PAD para el tratamiento del SDRA resultante de la COVID-19. La determinación del punto final primario se realizará al final del período de estudio principal de 28 días. El seguimiento de la seguridad y la supervivencia se llevará a cabo en las semanas 8, 26 y 52. También se ha presentado una autorización de ensayo clínico (CTA) en Europa para un ensayo COVID-19 de fase II, con los primeros sitios clínicos europeos planificados en Alemania e Italia.
“Estamos muy contentos de obtener la autorización para comenzar nuestro estudio de Fase II COVID-19 en los EUA. Hicimos un cambio de velocidad ahora con un enfoque principal en un inicio rápido del ensayo clínico, aprovechando nuestras ventajas competitivas tecnológicas y logísticas desarrolladas a través de la experiencia de nuestro ensayo clínico en los Estados Unidos y Europa. Creemos que podemos completar la inscripción rápidamente y esperamos proporcionar pautas sobre la duración esperada del estudio unas semanas después que comience”, dijo el director ejecutivo y Presidente de Pluristem, Yaky Yanay. “En las últimas semanas, hemos recibido docenas de solicitudes de médicos y familias que buscan participar en el programa de acceso ampliado por paciente. Esperamos trabajar con hospitales y médicos a mayor escala para entregar nuestras células PLX, a través de un candidato a producto comercial fácil de usar, que puede acelerar el tiempo de recuperación de condiciones que amenazan la vida y mejorar la supervivencia, en los casos más graves de COVID-19”.
Enlace relacionado:
Pluristem Therapeutics Inc.
Las células PLX son células alogénicas de tipo mesenquimatoso que tienen propiedades inmunomoduladoras que inducen las células T reguladoras naturales del sistema inmune y los macrófagos M2 y, por lo tanto, pueden prevenir o revertir la activación exagerada peligrosa del sistema inmune. Los hallazgos preclínicos previos de las células PLX revelaron un beneficio terapéutico en estudios con animales de hipertensión pulmonar, fibrosis pulmonar, lesión renal aguda y lesión gastrointestinal, que son posibles complicaciones de la infección grave por COVID-19. Los datos clínicos con el uso de células PLX demostraron la fuerte potencia inmunomoduladora de las células PLX en pacientes después de una cirugía importante.
Las celdas PLX están disponibles en el mercado y una vez comercializadas, se pueden fabricar en grandes cantidades. Pluristem cree que sus células PLX ofrecerán una ventaja clave para abordar la pandemia global de COVID-19. Las células PLX podrían reducir potencialmente la incidencia y/o la gravedad de la neumonía y neumonitis por COVID-19, lo que con suerte mejoraría el pronóstico de los pacientes. Las capacidades potenciales de las células PLX, junto con el perfil de seguridad observado en los ensayos clínicos que involucran a cientos de pacientes en todo el mundo, las posicionan potencialmente como una terapia para mitigar los efectos dañinos de la COVID-19 en los tejidos.
El estudio de fase II, titulado “Un estudio aleatorizado de fase II, doble ciego, controlado con placebo, multicéntrico, de grupos paralelos, para evaluar la eficacia y seguridad de las inyecciones intramusculares de PLX-PAD para el tratamiento de COVID-19 grave” tratará 140 pacientes adultos intubados y ventilados mecánicamente y que sufren insuficiencia respiratoria y SDRA debido a COVID-19. El criterio de valoración principal de eficacia del estudio es el número de días sin ventilador durante los 28 días desde el día uno hasta el día 28 del estudio.
El objetivo del estudio es evaluar la eficacia y seguridad de una o dos inyecciones intramusculares (IM), en tres dosis diferentes, de PLX-PAD para el tratamiento del SDRA resultante de la COVID-19. La determinación del punto final primario se realizará al final del período de estudio principal de 28 días. El seguimiento de la seguridad y la supervivencia se llevará a cabo en las semanas 8, 26 y 52. También se ha presentado una autorización de ensayo clínico (CTA) en Europa para un ensayo COVID-19 de fase II, con los primeros sitios clínicos europeos planificados en Alemania e Italia.
“Estamos muy contentos de obtener la autorización para comenzar nuestro estudio de Fase II COVID-19 en los EUA. Hicimos un cambio de velocidad ahora con un enfoque principal en un inicio rápido del ensayo clínico, aprovechando nuestras ventajas competitivas tecnológicas y logísticas desarrolladas a través de la experiencia de nuestro ensayo clínico en los Estados Unidos y Europa. Creemos que podemos completar la inscripción rápidamente y esperamos proporcionar pautas sobre la duración esperada del estudio unas semanas después que comience”, dijo el director ejecutivo y Presidente de Pluristem, Yaky Yanay. “En las últimas semanas, hemos recibido docenas de solicitudes de médicos y familias que buscan participar en el programa de acceso ampliado por paciente. Esperamos trabajar con hospitales y médicos a mayor escala para entregar nuestras células PLX, a través de un candidato a producto comercial fácil de usar, que puede acelerar el tiempo de recuperación de condiciones que amenazan la vida y mejorar la supervivencia, en los casos más graves de COVID-19”.
Enlace relacionado:
Pluristem Therapeutics Inc.
Últimas COVID-19 noticias
- Sistema de bajo costo detecta el virus SARS-CoV-2 en el aire del hospital mediante burbujas de alta tecnología
- China aprueba la primera vacuna inhalable contra la COVID-19 del mundo
- Vacuna en parche contra la COVID-19 combate variantes del SARS-CoV-2 mejor que las agujas
- Pruebas de viscosidad sanguínea predicen riesgo de muerte en pacientes hospitalizados con COVID-19
- ‘Computadora Covid’ usa IA para detectar COVID-19 en exámenes de TC de tórax
- Técnica de resonancia magnética muestra la causa de los síntomas de COVID prolongada
- TC del tórax de los pacientes con COVID-19 podrían ayudar a diferenciar entre las variantes del SARS-CoV-2
- Resonancia magnética especializada detecta anormalidades pulmonares en pacientes no hospitalizados con COVID prolongada
- Algoritmo de IA identifica a los pacientes hospitalizados con mayor riesgo de morir por COVID-19
- Estudio evalúa el impacto de la COVID-19 sobre la gammagrafía de ventilación/perfusión
- Sensor de sudor detecta biomarcadores claves que suministran una alarma precoz de la COVID-19 y la influenza
- Modelo de IA para seguimiento de COVID-19 predice mortalidad durante los primeros 30 días del ingreso
- ECG puede señalar pacientes hospitalizados con COVID-19 con riesgo más alto de muerte
- IA predice pronóstico de COVID a un nivel casi experto con base en tomografías computarizadas
- Examen de TC muestra evidencia de daño pulmonar persistente mucho tiempo después de neumonía por COVID-19
- Plataforma órgano-en-un-chip ayuda a diseñar estrategia para tratar complicaciones severas de la COVID-19
Canales
Cuidados Criticos
ver canal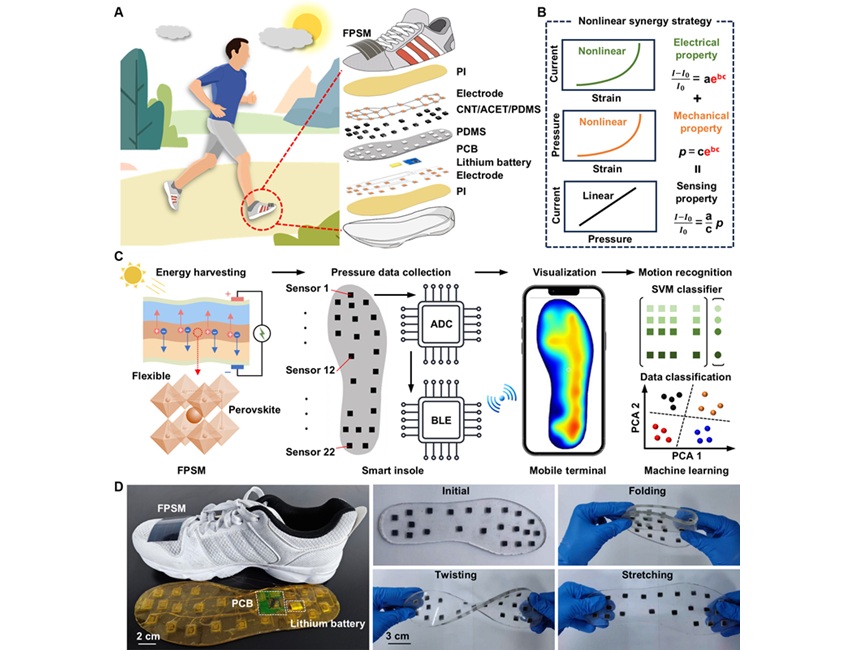
Plantilla inteligente inalámbrica y autoalimentada mejora el control de la salud personal
Millones de personas enfrentan dificultades con funciones ambulatorias, como caminar, correr y subir escaleras. Aunque en los últimos años ha crecido el interés por desarrollar sistemas... MásNovedoso sistema de cánula permite la administración dirigida de agentes de imagen y fármacos
La microscopía multifotónica se ha convertido en una herramienta invaluable en neurociencia, permitiendo a los investigadores observar la actividad cerebral en tiempo real con imágenes... MásTécnicas Quirúrgicas
ver canal
Tecnología de bypass coronario sin suturas elimina la necesidad de cirugías a corazón abierto
En pacientes con enfermedad de las arterias coronarias, ciertos vasos sanguíneos pueden estar estrechados o bloqueados, lo que requiere la colocación de un stent o la realización de... Más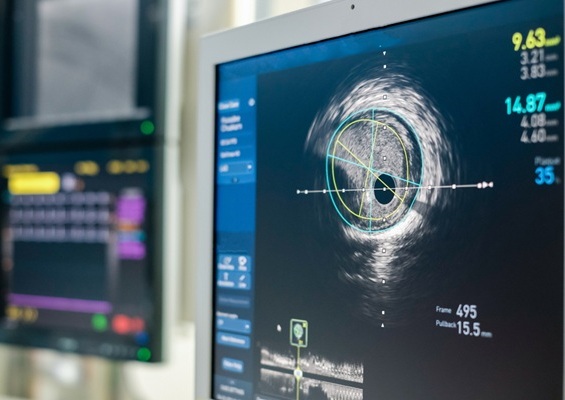
Las imágenes intravasculares mejoran la seguridad en la implantación de stents
Los pacientes diagnosticados con enfermedad coronaria arterial, causada por la acumulación de placa en las arterias, se someten con frecuencia a una intervención coronaria percutánea (ICP).... MásCuidados de Pacientes
ver canal
Plataforma de biosensores portátiles reducirá infecciones adquiridas en el hospital
En la Unión Europea, aproximadamente 4 millones de pacientes adquieren infecciones asociadas a la atención de la salud (IAAS), o infecciones nosocomiales, cada año, lo que provoca alrededor de 37.... MásTecnología portátil de luz germicida, única en su tipo, desinfecta superficies clínicas de alto contacto en segundos
La reducción de las infecciones adquiridas en la atención sanitaria (IAAS) sigue siendo una cuestión apremiante dentro de los sistemas sanitarios mundiales. Sólo en Estados Unidos, 1,7 millones de pacientes... Más
Solución de optimización de la capacidad quirúrgica ayuda a hospitales a impulsar utilización de quirófanos
Una solución innovadora tiene la capacidad de transformar la utilización de la capacidad quirúrgica al atacar la causa raíz de las ineficiencias los bloques de tiempo quirúrgico.... Más
Innovación revolucionaria en esterilización de instrumentos quirúrgicos mejora significativamente rendimiento del quirófano
Una innovación revolucionaria permite a los hospitales mejorar significativamente el tiempo de procesamiento de instrumentos y el rendimiento en quirófanos y departamentos de procesamiento... MásTI
ver canal
Nanopartículas imprimibles permiten la producción masiva de biosensores portátiles
Es probable que el futuro de la medicina se centre en la personalización de la atención médica, comprendiendo exactamente lo que cada individuo necesita y proporcionando la combinación... Más
Los relojes inteligentes podrían detectar la insuficiencia cardíaca congestiva
El diagnóstico de la insuficiencia cardíaca congestiva (ICC) suele requerir técnicas de diagnóstico por imagen costosas y que consumen mucho tiempo, como la ecocardiografía,... MásPruebas POC
ver canal
Lector de inmunoensayo de pruebas POC proporciona análisis cuantitativo de kits de prueba para diagnóstico más preciso
Un lector de inmunoensayos cuantitativos pequeño y liviano que proporciona un análisis cuantitativo de cualquier tipo de kits o tiras de prueba rápida, y se puede conectar a una PC... Más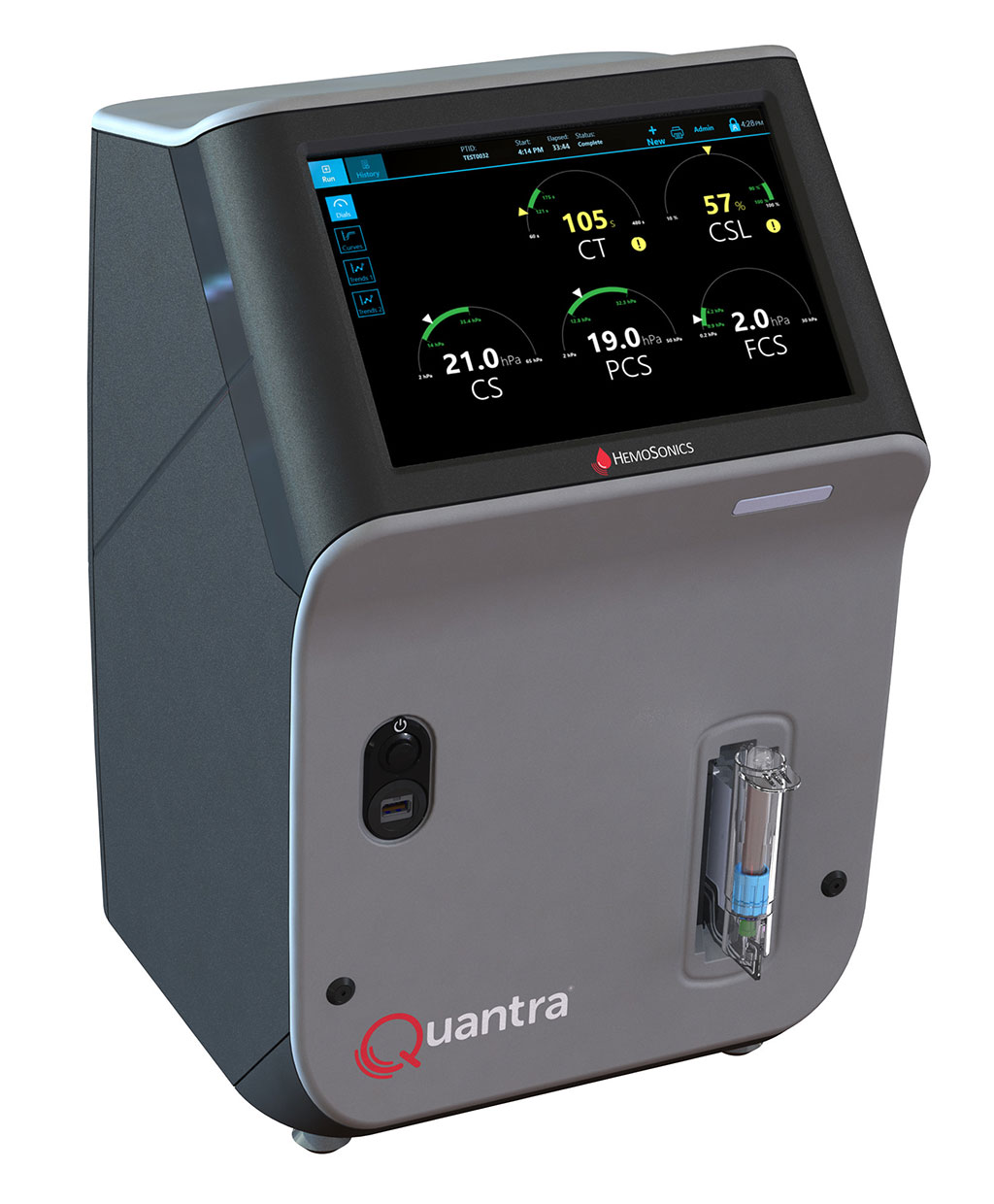
Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
Las pruebas hemostáticas actuales proporcionan solo un subconjunto de la información necesaria, o tardan demasiado en ser útiles en situaciones críticas de hemorragia, lo que... Más
Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
La resistencia a los antimicrobianos (RAM) es la falta de respuesta de las bacterias a un determinado antibiótico debido a mutaciones o genes de resistencia que la especie ha adquirido.... MásNegocios
ver canal
Colaboración ampliada transformará la tecnología en quirófanos mediante IA y automatización
La expansión de una colaboración existente entre tres empresas líderes tiene como objetivo desarrollar soluciones impulsadas por inteligencia artificial (IA) para quirófanos... Más