Presión acústica ayuda a suministrar medicamentos al cerebro
|
Por el equipo editorial de HospiMedica en español Actualizado el 22 Sep 2014 |
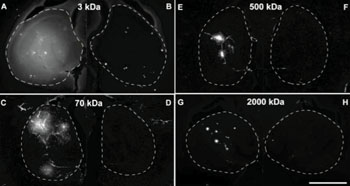
Imagen: Imágenes de fluorescencia de un hipocampo murino después de la difusión del dextrano a través de la BHE abierta mediante el FUS (izquierda), en comparación con la contralateral que muestra que no hay captación (derecha) (Fotografía cortesía de la Dra. Elisa Konofagou / Universidad de Columbia).
Una nueva técnica usa un rayo de ultrasonido enfocado (FUS) para controlar el tamaño de las moléculas que penetran la barrera hemato-encefálica (BHE).
Investigadores de la Universidad de Columbia (Nueva York, NY, EUA), realizaron un estudio que aplicó FUS a un hipocampo de ratón en presencia de microburbujas administradas por vía sistémica (MBs) que contienen dextranos marcados con fluorescencia, con pesos moleculares de 3-2,000 kDa (2,3 a 54,4 nm de diámetro), para examinar la posibilidad de poder suministrar los medicamentos a través de la BHE usando dextrano. Los resultados fueron evaluados utilizando imágenes ex vivo de fluorescencia, y la detección de cavitación fue empleada para monitorizar simultáneamente la actividad de las MB, asociada con el suministro de los dextranos.
Los resultados mostraron que la apertura inducida en la BHE por el FUS, definido por el tamaño de la molécula más grande que puede penetrar a través de la BHE, puede ser controlado mediante la presión acústica. El tamaño de la abertura en la BHE era inferior a 3 kDa (2,3 nm) a 0,31 MPa y alcanzó los 70 kDa (10,2 nm) a 0,51 MPa, y era tan grande como 2000 kDa (54,4 nm) a 0,84 MPa. El tamaño de la abertura relativamente pequeña (hasta 70 kDa) se logró con sólo cavitación estable; Sin embargo, la cavitación inercial se asoció con un tamaño relativamente mayor de la abertura en la BHE (por encima de 500 kDa). El estudio fue publicado en la edición de julio 2014 de la revista Journal of Cerebral Blood Flow & Metabolism.
“Actualmente, la mayoría de los medicamentos de moléculas pequeñas y grandes no penetran la barrera hemato-encefálica que se encuentra entre el lecho vascular y el tejido cerebral”, dijo la coautora del estudio, la profesor de ingeniería biomédica y radiología, Elisa Konofagou, PhD, de Ingeniería de Columbia. “Este es un avance importante para lograr que los medicamentos logren penetrar a partes específicas del cerebro con precisión, de forma no invasiva, y con seguridad, y puede ayudar en el tratamiento de enfermedades del sistema nervioso central como la enfermedad de Parkinson y la enfermedad de Alzheimer”.
El FUS en conjunto con las burbujas MBs, unas burbujas llenas de gas recubiertas por proteínas o lípidos, es hasta ahora la única técnica que puede permear la BHE de forma segura y no invasiva. Cuando las MBs son golpeadas por un rayo FUS, empiezan a oscilar debido a la cavitación, formando cavidades de vapor en la fase líquida; dependiendo de la magnitud de la presión, siguen oscilando o colapsan. El estudio mostró que la presión de la FUS se puede ajustar dependiendo del tamaño del medicamento que debe ser suministrado al cerebro - moléculas pequeñas a presiones más bajas y las moléculas más grandes a presiones más altas.
Enlace relacionado:
Columbia University
Investigadores de la Universidad de Columbia (Nueva York, NY, EUA), realizaron un estudio que aplicó FUS a un hipocampo de ratón en presencia de microburbujas administradas por vía sistémica (MBs) que contienen dextranos marcados con fluorescencia, con pesos moleculares de 3-2,000 kDa (2,3 a 54,4 nm de diámetro), para examinar la posibilidad de poder suministrar los medicamentos a través de la BHE usando dextrano. Los resultados fueron evaluados utilizando imágenes ex vivo de fluorescencia, y la detección de cavitación fue empleada para monitorizar simultáneamente la actividad de las MB, asociada con el suministro de los dextranos.
Los resultados mostraron que la apertura inducida en la BHE por el FUS, definido por el tamaño de la molécula más grande que puede penetrar a través de la BHE, puede ser controlado mediante la presión acústica. El tamaño de la abertura en la BHE era inferior a 3 kDa (2,3 nm) a 0,31 MPa y alcanzó los 70 kDa (10,2 nm) a 0,51 MPa, y era tan grande como 2000 kDa (54,4 nm) a 0,84 MPa. El tamaño de la abertura relativamente pequeña (hasta 70 kDa) se logró con sólo cavitación estable; Sin embargo, la cavitación inercial se asoció con un tamaño relativamente mayor de la abertura en la BHE (por encima de 500 kDa). El estudio fue publicado en la edición de julio 2014 de la revista Journal of Cerebral Blood Flow & Metabolism.
“Actualmente, la mayoría de los medicamentos de moléculas pequeñas y grandes no penetran la barrera hemato-encefálica que se encuentra entre el lecho vascular y el tejido cerebral”, dijo la coautora del estudio, la profesor de ingeniería biomédica y radiología, Elisa Konofagou, PhD, de Ingeniería de Columbia. “Este es un avance importante para lograr que los medicamentos logren penetrar a partes específicas del cerebro con precisión, de forma no invasiva, y con seguridad, y puede ayudar en el tratamiento de enfermedades del sistema nervioso central como la enfermedad de Parkinson y la enfermedad de Alzheimer”.
El FUS en conjunto con las burbujas MBs, unas burbujas llenas de gas recubiertas por proteínas o lípidos, es hasta ahora la única técnica que puede permear la BHE de forma segura y no invasiva. Cuando las MBs son golpeadas por un rayo FUS, empiezan a oscilar debido a la cavitación, formando cavidades de vapor en la fase líquida; dependiendo de la magnitud de la presión, siguen oscilando o colapsan. El estudio mostró que la presión de la FUS se puede ajustar dependiendo del tamaño del medicamento que debe ser suministrado al cerebro - moléculas pequeñas a presiones más bajas y las moléculas más grandes a presiones más altas.
Enlace relacionado:
Columbia University
Últimas Cuidados Criticos noticias
- Tecnología innovadora combina detección y tratamiento de trastornos del sistema nervioso en un solo procedimiento.
- Irradiación de plasma promueve una cicatrización ósea más rápida
- Nuevo dispositivo trata la lesión renal aguda por sepsis
- La revascularización mejora la calidad de vida de pacientes con isquemia crónica que amenaza las extremidades
- Modelos de predicción basados en IA predicen con precisión el deterioro de pacientes en cuidados críticos
- PCI preventiva para placas coronarias de alto riesgo reduce los eventos cardíacos
- Herramienta de IA guía el diagnóstico rápido y la predicción de sepsis
- Primer sistema de alerta de sepsis impulsado por IA del mundo detecta sepsis en un minuto
- Nueva tecnología podría revolucionar atención de valvulopatías cardíacas
- Dispositivo electrónico portátil súper permeable permite monitorear bioseñales a largo plazo
- Nuevo hidrogel con capacidades mejoradas para tratar aneurismas y detener su progresión
- Nueva herramienta de IA predice eventos médicos para respaldar toma de decisiones clínicas en entornos de atención médica
- El magnetómetro de un teléfono inteligente utiliza hidrogel magnetizado para medir biomarcadores para el diagnóstico de enfermedades
- Malla bioelectrónica crece con tejidos cardíacos para monitorización cardíaca integral
- Procedimiento mínimamente invasivo ofrece última esperanza para pacientes que enfrentan amputación debido a enfermedad vascular grave
- Cápsula tragable podría transformar detección de enfermedades gastrointestinales
Canales
Técnicas Quirúrgicas
ver canal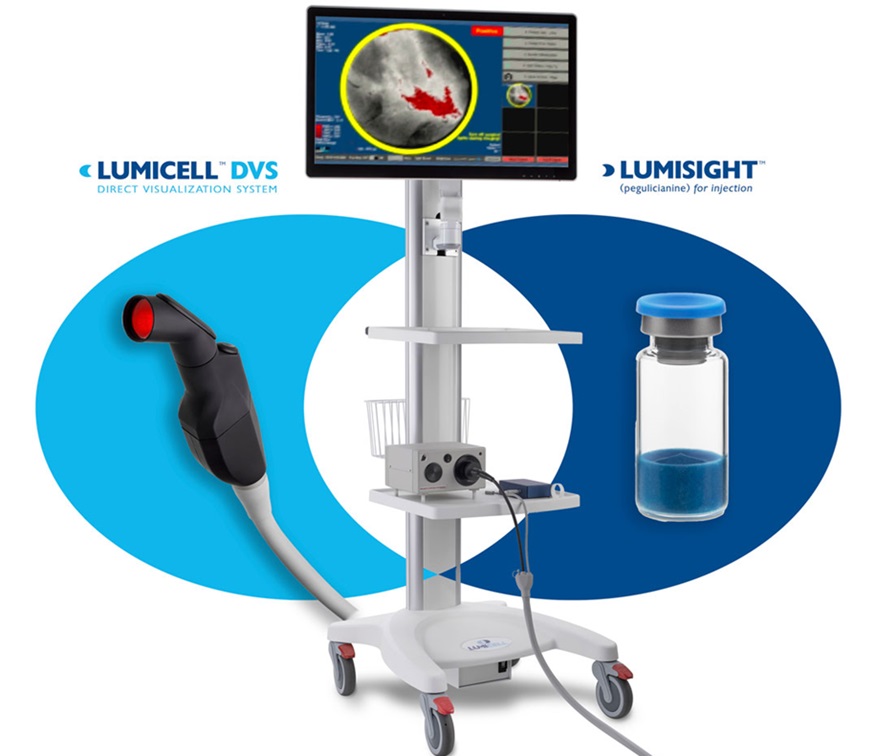
Plataforma de imágenes de vanguardia detecta cáncer de mama residual que no se detectó durante la cirugía de lumpectomía
El cáncer de mama es cada vez más común y las estadísticas indican que 1 de cada 8 mujeres desarrollará la enfermedad a lo largo de su vida. La lumpectomía sigue... Más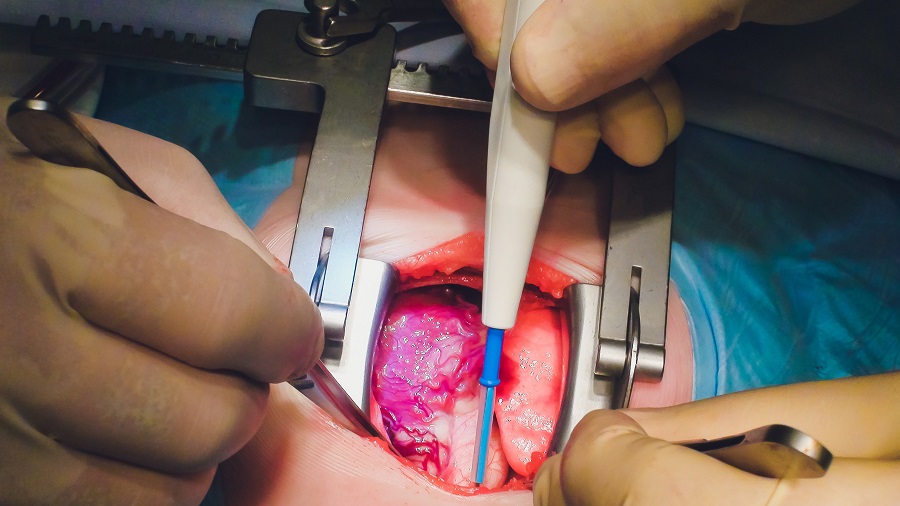
Modelos computacionales predicen la fuga de válvulas cardíacas en niños
El síndrome del corazón izquierdo hipoplásico es un defecto congénito grave en el que el lado izquierdo del corazón de un bebé está subdesarrollado y es... Más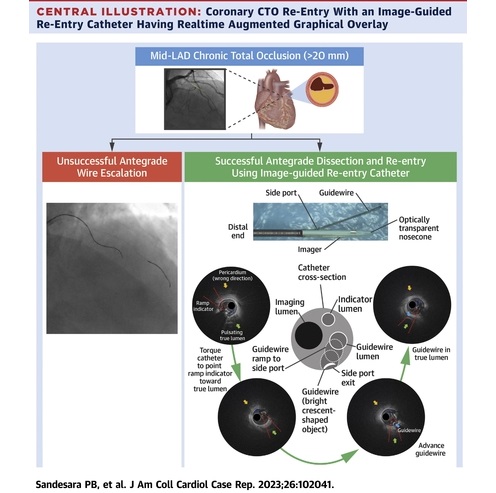
Dispositivo innovador permite orientación visual clara y en tiempo real para intervenciones cardiovasculares efectivas
La oclusión total crónica coronaria (OCT) es una afección en la que una arteria coronaria queda completamente bloqueada debido a la acumulación de placa. Aproximadamente entre... MásCuidados de Pacientes
ver canal
Solución de optimización de la capacidad quirúrgica ayuda a hospitales a impulsar utilización de quirófanos
Una solución innovadora tiene la capacidad de transformar la utilización de la capacidad quirúrgica al atacar la causa raíz de las ineficiencias los bloques de tiempo quirúrgico.... Más
Innovación revolucionaria en esterilización de instrumentos quirúrgicos mejora significativamente rendimiento del quirófano
Una innovación revolucionaria permite a los hospitales mejorar significativamente el tiempo de procesamiento de instrumentos y el rendimiento en quirófanos y departamentos de procesamiento... Más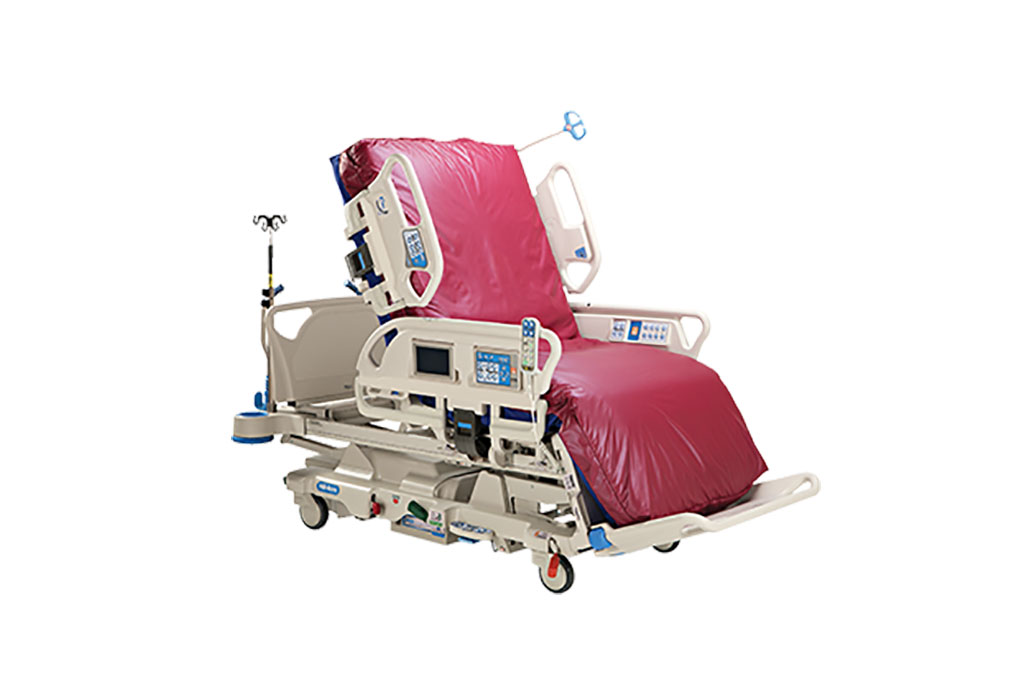
Cama para UCI de próxima generación ayuda a abordar necesidades complejas de cuidados intensivos
A medida que el entorno de cuidados intensivos se vuelve cada vez más exigente y complejo debido a las cambiantes necesidades de los hospitales, existe una necesidad apremiante de innovaciones que... MásTI
ver canal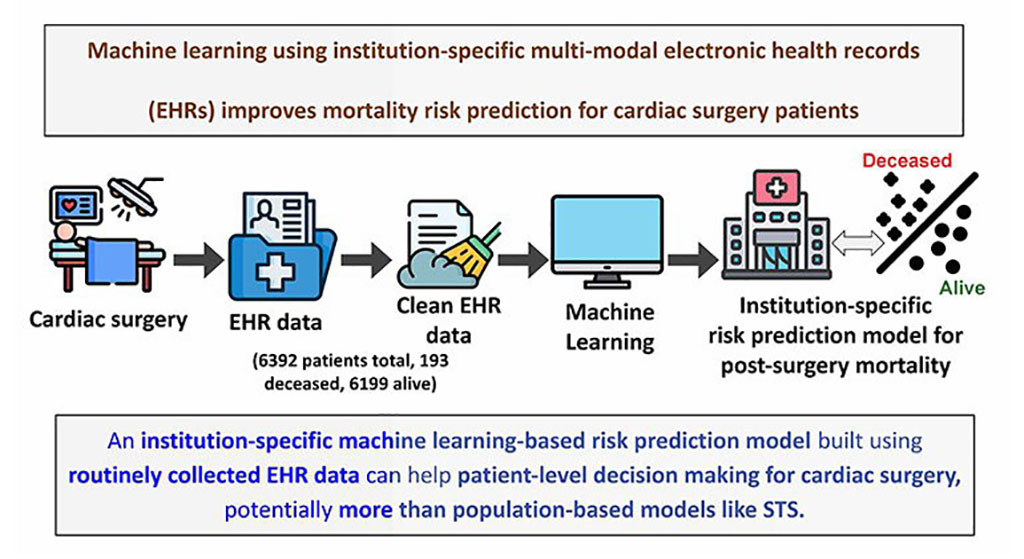
Modelo de aprendizaje automático mejora predicción del riesgo de mortalidad para pacientes de cirugía cardíaca
Se han implementado algoritmos de aprendizaje automático para crear modelos predictivos en varios campos médicos, y algunos han demostrado mejores resultados en comparación con sus... Más
Colaboración estratégica para desarrollar e integrar IA generativa en el cuidado de la salud
Los más altos expertos de la industria han subrayado el requisito inmediato de que los sistemas de salud y los hospitales respondan a las severas presiones de costos y márgenes.... MásPruebas POC
ver canal
Lector de inmunoensayo de pruebas POC proporciona análisis cuantitativo de kits de prueba para diagnóstico más preciso
Un lector de inmunoensayos cuantitativos pequeño y liviano que proporciona un análisis cuantitativo de cualquier tipo de kits o tiras de prueba rápida, y se puede conectar a una PC... Más
Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
Las pruebas hemostáticas actuales proporcionan solo un subconjunto de la información necesaria, o tardan demasiado en ser útiles en situaciones críticas de hemorragia, lo que... Más
Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
La resistencia a los antimicrobianos (RAM) es la falta de respuesta de las bacterias a un determinado antibiótico debido a mutaciones o genes de resistencia que la especie ha adquirido.... MásNegocios
ver canal
Johnson & Johnson adquiere la empresa de dispositivos médicos cardiovasculares Shockwave Medical
Johnson & Johnson (New Brunswick, Nueva Jersey, EUA) y Shockwave Medical (Santa Clara, CA, EUA.) han firmado un acuerdo definitivo en virtud del cual Johnson & Johnson adquirirá todas las... Más