Kit de prueba rápida IgG/IgM contra la COVID-19 de Healgen recibió autorización para uso en emergencias
|
Por el equipo editorial de HospiMedica en español Actualizado el 05 Jun 2020 |
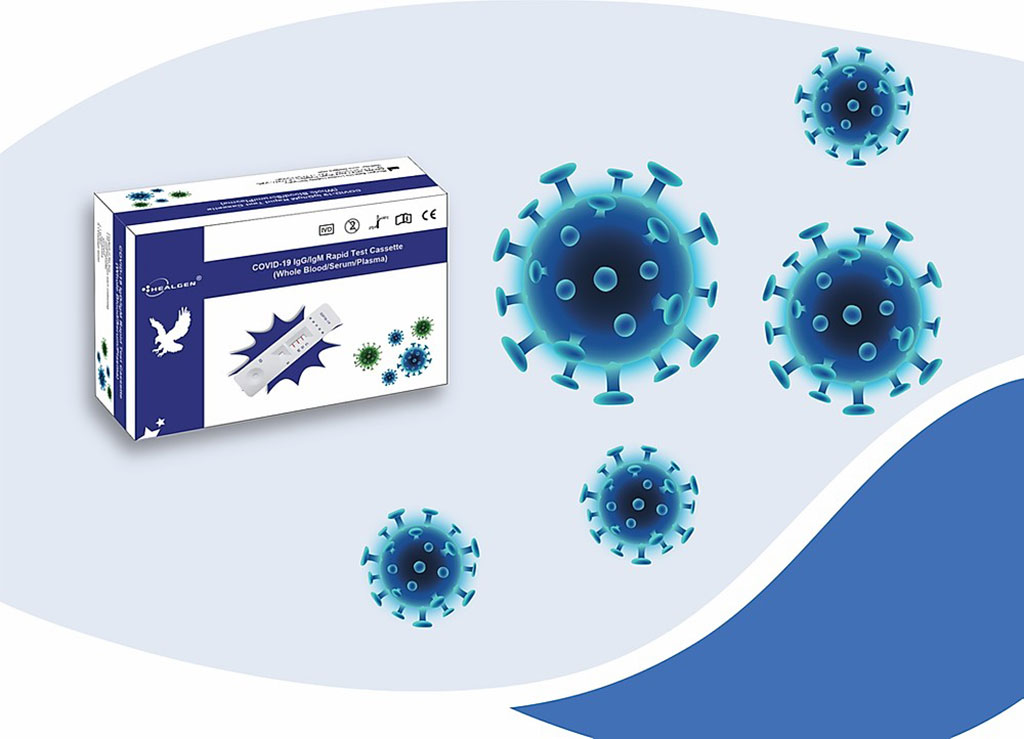
Imagen: El casete de prueba rápida Healgen COVID-19 IgG/IgM (Fotografía cortesía de Healgen Scientific, LLC)
El Kit de Prueba Rápida IgG/IgM COVID-19 de Healgen Scientific, LLC (Houston, TX, EUA) recibió la autorización de uso en emergencias (AUE) de la Administración de Medicamentos y Alimentos de los Estados Unidos (FDA).
Como resultado de la autorización de la FDA, Confirm BioSciences (San Diego, CA, EUA), el mayor distribuidor norteamericano de Healgen, una subsidiaria de Zhejiang Orient Gene Biotech, fabricante de la prueba para la COVID-19, tendrá un amplio suministro de kits de análisis para uso por profesionales médicos a partir de principios de junio. Confirm espera tener disponibilidad de millones de pruebas, suficientes para satisfacer los pedidos anticipados existentes y los pedidos futuros. Zhejiang también designó a Aytu BioScience, Inc. (Englewood, CO, EUA) como el distribuidor en EUA para la prueba para la COVID-19 y entregó más de 1,4 millones de pruebas rápidas a la compañía para su distribución en el país.
Los kits de prueba rápida COVID-19 IgG/IgM son kits de análisis fáciles de usar que proporcionan resultados en solo 10 minutos, diseñados para uso con muestras de sangre total, suero o plasma. Con un alto grado de exactitud, los kits detectan la IgM que puede aparecer en la sangre dentro de los tres y cinco días posteriores a la incubación y la IgG que aparece en apenas 1-2 semanas. Como parte de la revisión de la FDA, un estudio de los Institutos Nacionales de Salud (NIH) que comparó los kits de prueba rápida descubrió que la prueba rápida COVID-19 demostró un desempeño excelente. Las pruebas están autorizadas para uso con receta solo para su uso en laboratorios CLIA de alta o moderada complejidad. Los kits tienen una vida útil de 24 meses a partir de la fecha de fabricación y se pueden almacenar a temperatura ambiente o en un refrigerador.
“Hemos recibido comentarios positivos sobre la prueba, de nuestros clientes y de estudios independientes, por lo que la autorización para uso en emergencias de la FDA valida lo que ya sabíamos de las aplicaciones clínicas del mundo real”, dijo Albert Berger, director ejecutivo de Confirm BioSciences. “Esta pandemia es un desafío enorme para los profesionales médicos y para todos los demás y como distribuidor principal, estamos orgullosos de hacer nuestra parte para aumentar la capacidad de análisis para que los profesionales de la salud puedan ayudar a contener la propagación del virus”.
Enlace relacionado:
Healgen Scientific, LLC
Confirm BioSciences
Aytu BioScience, Inc.
Como resultado de la autorización de la FDA, Confirm BioSciences (San Diego, CA, EUA), el mayor distribuidor norteamericano de Healgen, una subsidiaria de Zhejiang Orient Gene Biotech, fabricante de la prueba para la COVID-19, tendrá un amplio suministro de kits de análisis para uso por profesionales médicos a partir de principios de junio. Confirm espera tener disponibilidad de millones de pruebas, suficientes para satisfacer los pedidos anticipados existentes y los pedidos futuros. Zhejiang también designó a Aytu BioScience, Inc. (Englewood, CO, EUA) como el distribuidor en EUA para la prueba para la COVID-19 y entregó más de 1,4 millones de pruebas rápidas a la compañía para su distribución en el país.
Los kits de prueba rápida COVID-19 IgG/IgM son kits de análisis fáciles de usar que proporcionan resultados en solo 10 minutos, diseñados para uso con muestras de sangre total, suero o plasma. Con un alto grado de exactitud, los kits detectan la IgM que puede aparecer en la sangre dentro de los tres y cinco días posteriores a la incubación y la IgG que aparece en apenas 1-2 semanas. Como parte de la revisión de la FDA, un estudio de los Institutos Nacionales de Salud (NIH) que comparó los kits de prueba rápida descubrió que la prueba rápida COVID-19 demostró un desempeño excelente. Las pruebas están autorizadas para uso con receta solo para su uso en laboratorios CLIA de alta o moderada complejidad. Los kits tienen una vida útil de 24 meses a partir de la fecha de fabricación y se pueden almacenar a temperatura ambiente o en un refrigerador.
“Hemos recibido comentarios positivos sobre la prueba, de nuestros clientes y de estudios independientes, por lo que la autorización para uso en emergencias de la FDA valida lo que ya sabíamos de las aplicaciones clínicas del mundo real”, dijo Albert Berger, director ejecutivo de Confirm BioSciences. “Esta pandemia es un desafío enorme para los profesionales médicos y para todos los demás y como distribuidor principal, estamos orgullosos de hacer nuestra parte para aumentar la capacidad de análisis para que los profesionales de la salud puedan ayudar a contener la propagación del virus”.
Enlace relacionado:
Healgen Scientific, LLC
Confirm BioSciences
Aytu BioScience, Inc.
Últimas COVID-19 noticias
- Sistema de bajo costo detecta el virus SARS-CoV-2 en el aire del hospital mediante burbujas de alta tecnología
- China aprueba la primera vacuna inhalable contra la COVID-19 del mundo
- Vacuna en parche contra la COVID-19 combate variantes del SARS-CoV-2 mejor que las agujas
- Pruebas de viscosidad sanguínea predicen riesgo de muerte en pacientes hospitalizados con COVID-19
- ‘Computadora Covid’ usa IA para detectar COVID-19 en exámenes de TC de tórax
- Técnica de resonancia magnética muestra la causa de los síntomas de COVID prolongada
- TC del tórax de los pacientes con COVID-19 podrían ayudar a diferenciar entre las variantes del SARS-CoV-2
- Resonancia magnética especializada detecta anormalidades pulmonares en pacientes no hospitalizados con COVID prolongada
- Algoritmo de IA identifica a los pacientes hospitalizados con mayor riesgo de morir por COVID-19
- Estudio evalúa el impacto de la COVID-19 sobre la gammagrafía de ventilación/perfusión
- Sensor de sudor detecta biomarcadores claves que suministran una alarma precoz de la COVID-19 y la influenza
- Modelo de IA para seguimiento de COVID-19 predice mortalidad durante los primeros 30 días del ingreso
- ECG puede señalar pacientes hospitalizados con COVID-19 con riesgo más alto de muerte
- IA predice pronóstico de COVID a un nivel casi experto con base en tomografías computarizadas
- Examen de TC muestra evidencia de daño pulmonar persistente mucho tiempo después de neumonía por COVID-19
- Plataforma órgano-en-un-chip ayuda a diseñar estrategia para tratar complicaciones severas de la COVID-19
Canales
Cuidados Criticos
ver canal
Innovador tratamiento inhalable para la TB ayuda a reducir los efectos secundarios
La tuberculosis (TB) sigue siendo una de las enfermedades infecciosas más mortales del mundo, a pesar de ser curable. El tratamiento requiere meses de múltiples fármacos que pueden causar efectos secundarios... Más
Algoritmo de IA mejora la toma de decisiones sobre antibióticos en infecciones del tracto urinario
Las infecciones del tracto urinario (ITU) se encuentran entre las infecciones bacterianas más comunes a nivel mundial y son un factor importante en el uso de antibióticos. La prescripción... Más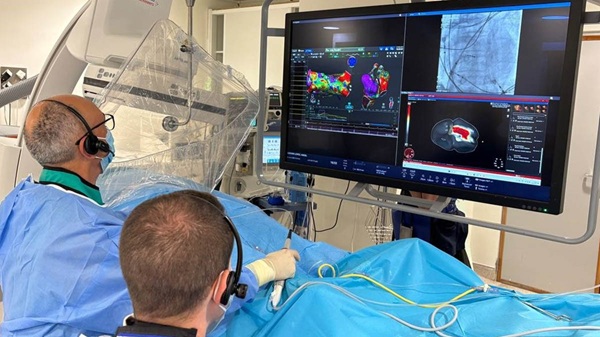
Tecnología de mapeo de corazón completo ofrece una visión integral de las arritmias cardíacas en un solo latido
Las arritmias cardíacas pueden ser difíciles de diagnosticar y tratar debido a que los sistemas de mapeo actuales analizan el corazón cámara por cámara.... Más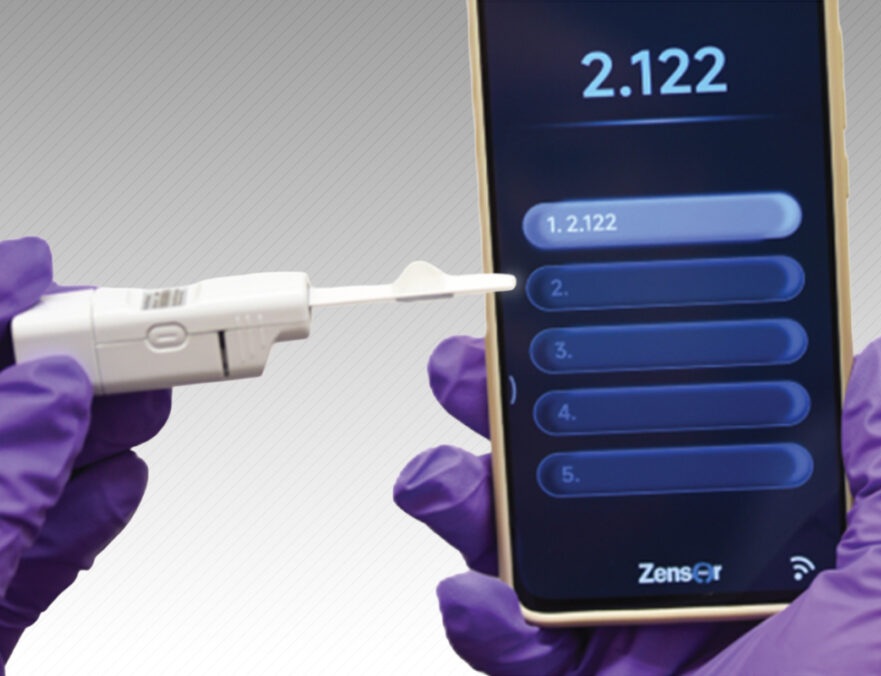
Dispositivo portátil para diabéticos podría reemplazar los sistemas de monitorización continua de glucosa
Monitorear la glucemia es esencial para las personas con diabetes a fin de prevenir complicaciones y mantener una salud a largo plazo. Los sistemas actuales de monitorización continua de la glucosa requieren... MásTécnicas Quirúrgicas
ver canal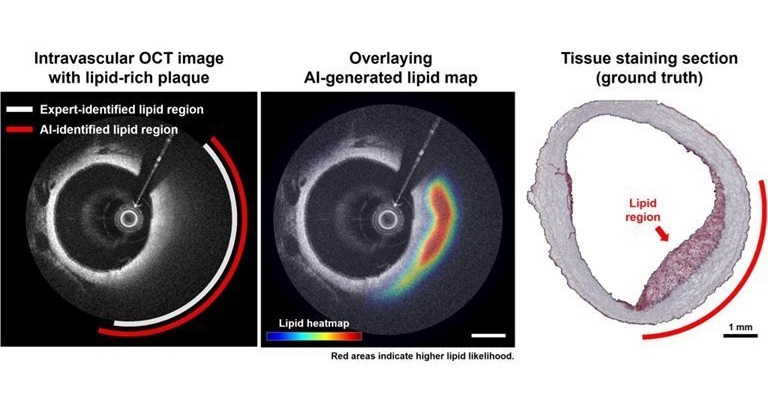
Análisis de imágenes OCT basado en IA identifica placas de alto riesgo en arterias coronarias
Las placas ricas en lípidos dentro de las arterias coronarias están fuertemente asociadas con ataques cardíacos y otros eventos cardíacos mayores. Si bien la tomografía... Más
Dispositivo neural estimula la regeneración del cráneo tras implante cerebral
La colocación de implantes electrónicos en el cerebro suele requerir la extirpación de una parte del cráneo, lo que dificulta el acceso a largo plazo y el cierre seguro. Los métodos actuales suelen implicar... MásCuidados de Pacientes
ver canal
Dispositivo automático de lavado de vías intravenosas mejora la atención en infusiones
Más del 80% de los pacientes hospitalizados reciben terapia intravenosa (IV). Cada dosis de medicamento IV administrada en una bolsa de infusión de pequeño volumen (<250 mL) debe... Más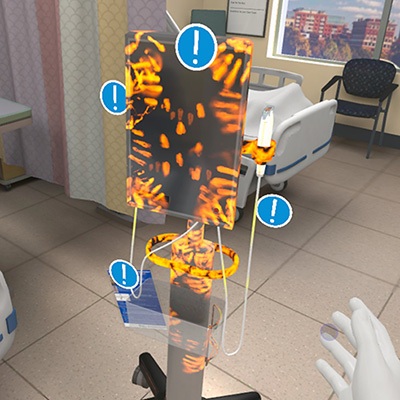
Herramienta de capacitación en realidad virtual combate la contaminación de equipos médicos portátiles
Las infecciones asociadas a la atención médica (IAAS) afectan a uno de cada 31 pacientes, causan casi 100.000 muertes al año y generan un costo de 28.4 mil millones de dólares... Más
Plataforma de biosensores portátiles reducirá infecciones adquiridas en el hospital
En la Unión Europea, aproximadamente 4 millones de pacientes adquieren infecciones asociadas a la atención de la salud (IAAS), o infecciones nosocomiales, cada año, lo que provoca alrededor de 37.... MásTecnología portátil de luz germicida, única en su tipo, desinfecta superficies clínicas de alto contacto en segundos
La reducción de las infecciones adquiridas en la atención sanitaria (IAAS) sigue siendo una cuestión apremiante dentro de los sistemas sanitarios mundiales. Sólo en Estados Unidos, 1,7 millones de pacientes... MásTI
ver canal
Herramienta basada en HCE predice el fallo del injerto tras un trasplante de riñón
El trasplante de riñón ofrece a los pacientes con enfermedad renal terminal una mayor supervivencia y mejor calidad de vida que la diálisis. Sin embargo, el fallo del injerto sigue... Más
Nanopartículas imprimibles permiten la producción masiva de biosensores portátiles
Es probable que el futuro de la medicina se centre en la personalización de la atención médica, comprendiendo exactamente lo que cada individuo necesita y proporcionando la combinación... MásPruebas POC
ver canal
Lector de inmunoensayo de pruebas POC proporciona análisis cuantitativo de kits de prueba para diagnóstico más preciso
Un lector de inmunoensayos cuantitativos pequeño y liviano que proporciona un análisis cuantitativo de cualquier tipo de kits o tiras de prueba rápida, y se puede conectar a una PC... Más
Sistema de hemostasia de sangre total POC de última generación reconoce necesidades específicas de servicios de emergencia y quirófanos
Las pruebas hemostáticas actuales proporcionan solo un subconjunto de la información necesaria, o tardan demasiado en ser útiles en situaciones críticas de hemorragia, lo que... Más
Laboratorio portátil permitirá identificación de infecciones bacterianas más rápida y económica en el punto de necesidad
La resistencia a los antimicrobianos (RAM) es la falta de respuesta de las bacterias a un determinado antibiótico debido a mutaciones o genes de resistencia que la especie ha adquirido.... MásNegocios
ver canal
Philips y Masimo se asocian para impulsar las tecnologías de monitorización de pacientes
Royal Philips (Ámsterdam, Países Bajos) y Masimo (Irvine, CA, EUA) han renovado su colaboración estratégica plurianual, combinando la experiencia de Philips en monitorización... Más